

发表期刊:Nature Metabolism
影响因子:19.865
作者单位:中山大学第一附属医院
能够快速无限地生长和分裂是癌细胞最广为人知的特征之一,癌细胞核糖体生物合成失调以及mRNA翻译活性异常,均会促进癌症的进展,然而,癌症中核糖体生物生成失调的分子机制仍不清楚。
核糖体生物发生是一个高度协调的过程,最近的研究表明,不同的RNA转录后修饰在基因表达和癌症进展的调节中均发挥重要作用。rRNA占细胞总RNA的80%以上,并受到不同的修饰,但是对于rRNA修饰在调节癌症中的rRNA加工和功能中的功能和机制知之甚少。关于mRNA中m6A的修饰已经成为癌症进程的关键信号,而rRNA中m6A修饰的研究还有很多待揭示的问题。
为揭示METTL5介导的18S rRNA m6A修饰对决定细胞命运和生长的作用,让我们走入作者的研究故事。
1.METTL5和TRMT112在各种癌症中上调,并与不良预后相关
根据前人的报道在rRNA中存在两个酶METTL5和TRMT112分别催化18SrRNA上1832位(m6A1832)和28SrRNA上4220位(m6A4220)的甲基化修饰。为了探明m6A修饰在癌症进程中的作用,作者首先对TCGA数据进行了分析,发现包括HCC在大多数TCGA癌症类型中METTL5和TRMT112均显著上调(图1a-c),并且发现METTL5和TRMT112的高表达与肝癌患者的晚期病理分级、肿瘤分期、总体生存率均相关(图1e-h)。为了进一步确定上述现象,作者在HCC细胞系以及HCC组织样本中做了进一步确认,正如预期的那样,无论在细胞系还是组织样本中,相较于对照组,METTL5和TRMT112的mRNA和蛋白水平均有不同程度的上调(图1i-m)。同时m6A定量检测也确认了,在HCC细胞系和HCC患者样本中m6A1832的修饰显著增高(图1n)。显然METTL5和TRMT112介导的18S rRNA m6A修饰很可能在HCC的进程中有重要的作用。
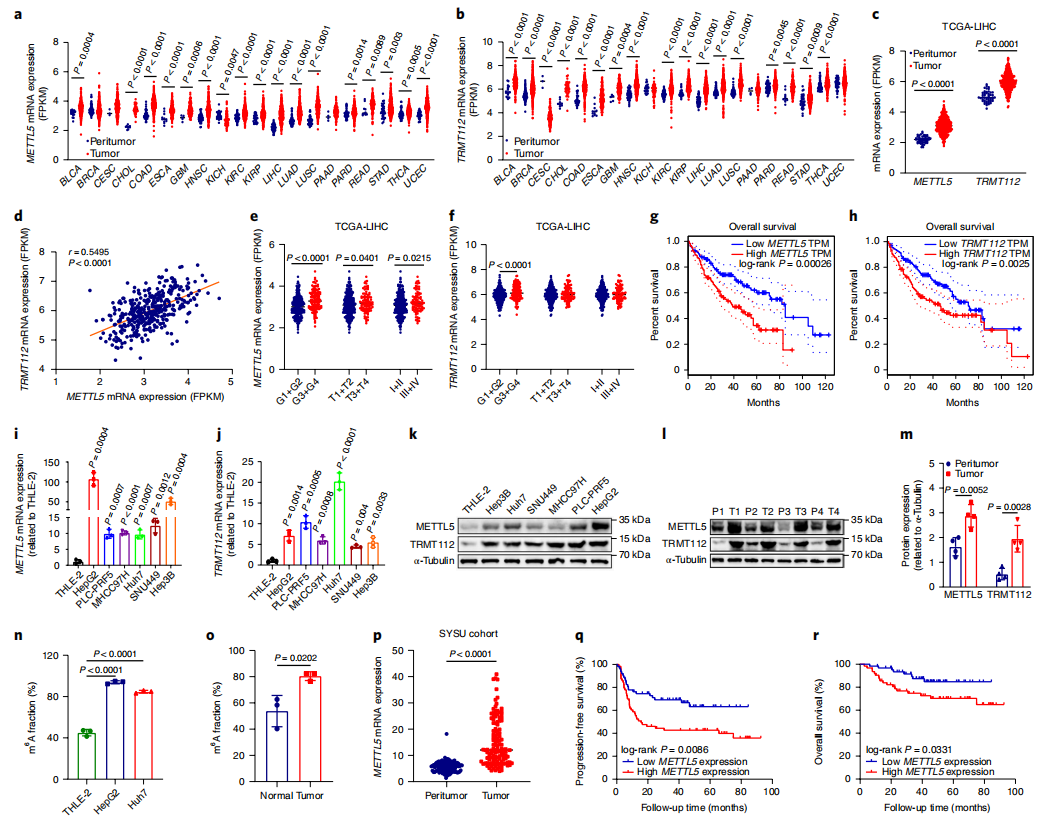
图1. MettL5在各种癌症中上调,并与低生存率相关
2.METTL5的过表达在体外和体内促进肝癌进展
为了深入研究METTL5的致癌功能,作者首先构建了METTL5过表达肝癌细胞系(图2a,b),显然METTL5的过表达显著的增加了HCC细胞中18S rRNA的m6A修饰(图2c)。不出意外的,METTL5的过表达从生长、迁移、侵袭等各方面促进了细胞系的活力(图2d-k)。表明METTL5可以在体外促进HCC的进展。
回到体内实验,METTL5的mRNA和蛋白质在METTL5过表达质粒转染的小鼠模型中均显著上调(图2l-n)。肿瘤形态检测与免疫组织化学实验同样从表型角度表明METTL5过表达的小鼠肿瘤有更高的增殖活性,综上所述,METTL5在体内体外均会促进HCC肿瘤的发生。
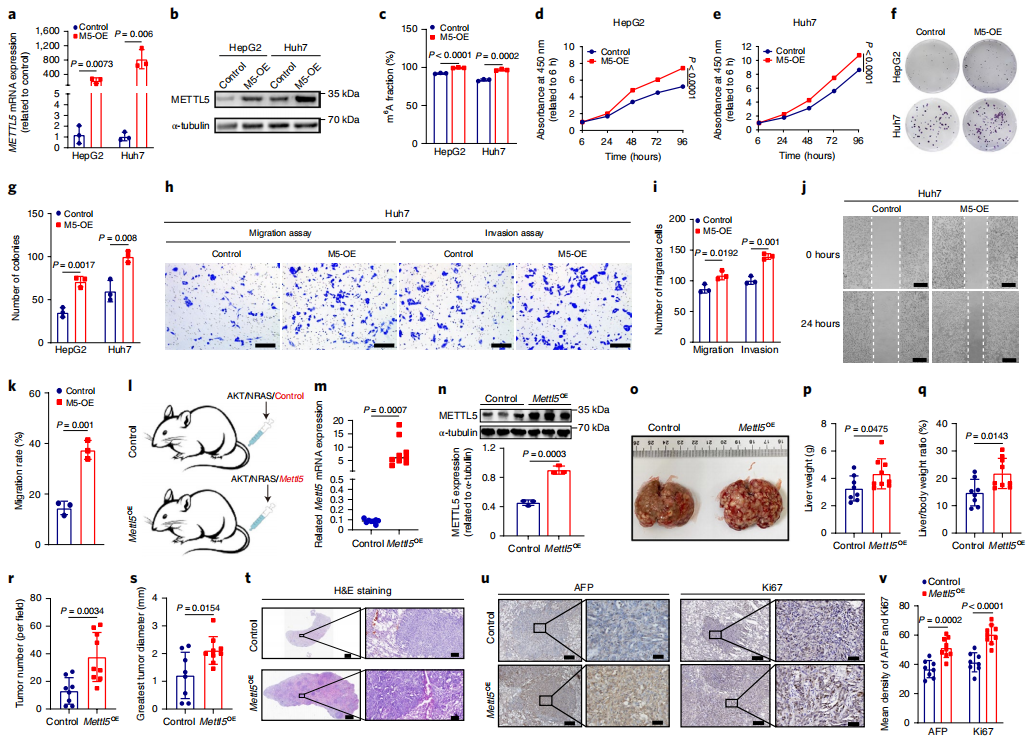
图2. MettL5的过表达在体外和体内促进肝癌的发生
3.METTL5介导的18S rRNA m6A修饰调节80S核糖体组装和全局mRNA翻译
为了全面分析METTL5在HCC中的功能,作者同样的对HCC细胞中的METTL5进行了敲低处理(图3a)。在体外试验中,METTL5敲低的处理使得HCC细胞的生长能力和集落形成能力均有所降低(图3b-d),除了增殖表型之外,METTL5的缺失对HCC的凋亡以及细胞周期均产生了不良的影响(图3e-l),结合上文的过表达数据,表明METTL5确实对HCC细胞起到了促进的作用。
作者进一步探究METTL5的作用机制,发现在METTL5缺失的细胞中,18S rRNA的m6A修饰显著减少(图3m),同时为了确定METTL5对18S rRNA的m6A的影响并非是通过影响18S rRNA表达量导致的,作者对18S rRNA表达量进行了检测(3图o)。18S rRNA是核糖体的主要成分,作者进一步研究METTL5对核糖体功能的影响机制,多聚体分析表明METTL5的敲减会使80S核糖体组装受损(图3q)。

图3. MettL5基因敲除体外抑制肝癌的发生
4.METTL5调节肝癌细胞的脂肪酸代谢
通过核糖体测序分析发现。受METTL5缺失影响的mRNA主要富集于非酒精性脂肪肝、脂肪酸生物合成等途径,表明METTL5对HCC进展的影响很可能与脂肪酸代谢重组相关(图4a-c)。脂质组学分析表明受METTL5敲除影响显著降低的脂质包括游离脂肪酸、甘油三酯、胆固醇(图4d-f)。为了确认这些受影响的脂质的来源信息,作者做了[U-13C]葡萄糖的代谢流分析,发现许多长链脂肪酸及其下游产物均被U-13C标记,表明这些脂肪酸来源于葡萄糖的生物合成,而随着METTL5的敲除,这些碳代谢产物的U-13C标记率显著降低了,显然METTL5影响了肝癌细胞中脂质代谢的重编程(图4h)。
作者进一步对长链脂肪酸进行LC-MS分析表明,大多数长链脂肪酸特别是多不饱和脂肪酸随着METTL5敲除显著降低,对代谢物进行富集分析发现,这些显著减少的多不饱和脂肪酸主要与β氧化途径相关(图4i-k),说明METTL5的缺失可能会损害细胞的β氧化。

图4. MettL5敲除损害脂肪酸β-氧化
5.ACSL4介导MettL5在脂肪酸代谢和肝癌进展中的功能
为了深入探究MettL5潜在的分子机制,作者分析了靶mRNA的特征,在富含脂肪酸代谢途径的mRNA中,酰基辅酶A合成酶长链家族(ACSL)成员,包括ACSL1、ACSL3、ACSL4和ACSL5,在缺乏METTL5的细胞中显示翻译效率降低,同样的METTL5缺乏的细胞中ACSL家族蛋白的表达水平也同步降低了(图5f)。
ACSL家族能够将长链脂肪酸转化脂肪酰基辅酶a酯,在癌症的长链脂肪代谢中起到至关重要的作用,为了分析ACSL在METTL5对HCC调控中的作用,作者在METTL5敲除的细胞中过表达的了ACSL4进行拯救实验。通过强制过表达ACSL4增加了细胞中的脂质水平(图5g-j)。同时细胞的增殖、集落形成、侵袭等能力均受ACSL4 表达而得到增强,(图5k-q),ACSL4 的强制表达同样的减少了HCC细胞的凋亡,并促进了细胞周期的进展(图5r-u)。上述实验说明,ACSL4的过表达可以在一定程度上挽救因MettL5缺失而受到的影响的癌症进展。为了研究结论的完整性,作者通过在MettL5过表达体系中敲除ACSL4,以及添加β氧化阻断剂的方式,证实了MettL5在肝癌中的致癌作用需要依赖ACSL4对脂肪酸β-氧化的调节作用。最后作者在小鼠体内同样的验证了上述现象。
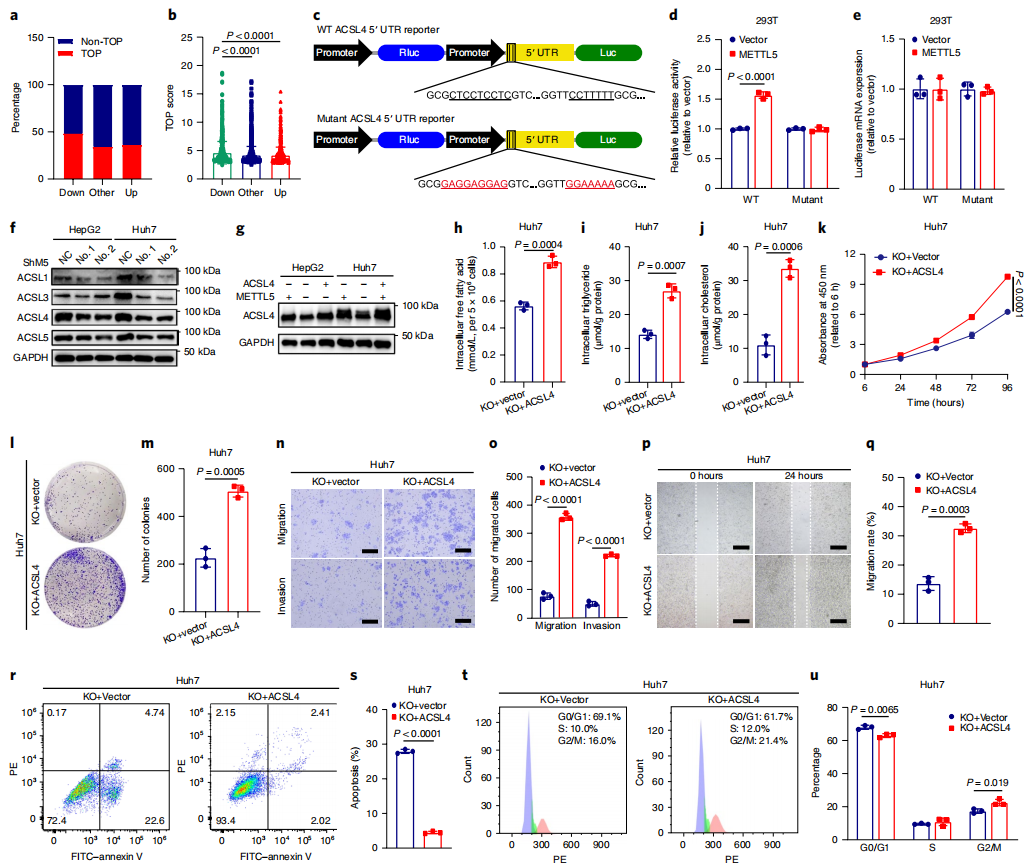
图5. ACSL4介导MettL5在脂肪酸代谢和肝癌进展中的功能
总的来说,本研究提供了强有力的体外和体内证据,支持METTL5介导的18S rRNA m6A修饰在肝癌中的致癌作用。此外,作者还进一步证明了rRNA表观遗传修饰、mRNA翻译和脂肪酸代谢之间的交联,为在转化水平上开发肝癌治疗的靶向治疗提供了有力的证据。
科研延伸
BIOTREE非靶代谢流解决方案:无偏向性的检测所有带同位素标记的代谢物,广泛筛选同位素标记的代谢物参与的代谢途径或基因敲除前、后代谢速率变化。

文献下载链接:
https://pan.baidu.com/s/1dfvufPYCeDu20aW_UjiyLA
提取码:0000









